40 процентный раствор формальдегида. Формалин - особенности применения. Способ применения и действие
Многие слышали о таком веществе, как формалин. Что это за химическое соединение? Его часто называют формолем. Оно является раствором формальдегида (36,5-40%). В качестве стабилизатора он содержит (4-12%). Эта бесцветная прозрачная жидкость имеет острый запах. Она может смешиваться со спиртом и водой в любых соотношениях.
Формалин: что это такое?
Это вещество чаще всего используется как дезинфицирующее средство. Его растворы (0,5-1%) используют для обмывания кожи при сильной потливости (ног, в подмышечных впадинах) и бромидрозе (резком Формалин эффективно снижает секрецию желез эпидермиса, но его нельзя использовать ежедневно. В некоторых случаях его используют для спринцевания (в концентрации 0,05%), промывания крипт миндалин (0,25%). Это вещество входит в состав препаратов «Лизоформ», «Формидрон», «Мазь формалиновая», «Паста Теймурова».
Побочные явления при использовании этого раствора: раздражение и пересушивание кожи, которое исчезает при смазывании ее жирным кремом или растительным маслом. Формалин, применение которого противопоказано при воспалительных процессах или раздражении эпидермиса, можно использовать только после их устранения.
Для дезинфекции медицинских инструментов и вещей пациентов также используют этот раствор. Применение в этом случае предусматривает только 0,5% формалин. Что это за препарат? Для использования в медицинских целях выпускают исключительно 10% раствор во флаконах из стекла объемом 100 мл. Хранят формалин в хорошо укупоренной таре в темном месте при температуре не меньше 9˚С. Это вещество считается токсичным для человека и животных.
Химический состав формалина

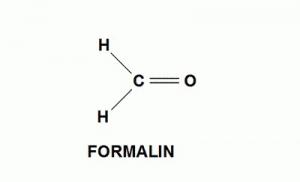
Как получается формалин? Формула этого вещества - СН 2 О. муравьиной кислоты), который является бесцветным газом с удушливым запахом, при охлаждении до -21 °С превращается в прозрачную жидкость. Температура его плавления составляет -92° С. При окислении он превращается в муравьиную кислоту. Формальдегид получается путем воздействия кислородом воздуха на метиловый спирт в виде паров в присутствии катализаторов. Из них особо продуктивным оказалось серебро, хотя в промышленности используется более доступная медь. Полученный перегон аккумулирует воду, в результате чего получается формалин. В нем могут содержаться примеси ацетона, уксусной или муравьиной кислоты. При упаривании формалина в остатке получается плотная масса полимеров, нерастворимых в холодной воде.
Свойства формалина

Это вещество вызывает необратимые изменения в протеинах протоплазмы. При этом оно некротизирует и мумифицирует ткани. При воздействии этого раствора на бактериальные клетки происходит денатурация их белков. В 5% формоле за 0,5 часа погибают споровые грибы. Под воздействием формалина гемоглобин крови становится метгемоглобином (продукт окисления ядами). При продолжительном хранении в холодном помещении этот раствор мутнеет. При этом образуется белесый осадок - параформальдегид.
Использование раствора формальдегида
Формалин используют как удобный источник формальдегида, применяемый в производстве поливинилформаля. Он также незаменим в качестве антисептического средства для дезинфекции помещений, инструментов, одежды, дубления кожевенного сырья. Его используют для бальзамирования органических веществ (организмов и органов). Формалин, применение которого для сохранения анатомических препаратов никого не удивляет, используют также в качестве фунгицида. Многие растениеводы протравливают этим раствором семена, клубни, корнеплоды перед посадкой и посевом.
Формалин, качество которого контролируется ГОСТ 1625-89, используется при изготовлении поверхностно-активных веществ, каучука, и некоторых других производных метилена. Раствор формальдегида используется также в текстильной промышленности. Он используется для улучшения потребительских свойств ткани по сопротивляемости к усадке и сминанию. В бумажной промышленности формалин улучшает качество бумаги и ее прочность.
Меры предосторожности при работе с формалином

При покупке этого вещества не стоит забывать о том, как может быть опасен формалин. Что это за предосторожности? хранения этого вещества со дня изготовления - 90 суток. Формалин продается во флаконах, канистрах, бочках. Раствор формальдегида нужно держать как можно дальше от детей. При приеме формалина внутрь появляется жжение и и желудке. После этого появляется рвота с кровью. Также при отравлении формалином возникает кашель, чихание, гипертермия слизистой глаз, одышка. Человек может испытывать судороги, головокружение, приступы паники. В некоторых случаях отравление формалином заканчивается летальным исходом, который наступает вследствие паралича дыхания и асфикции. Смертельная доза - 10-15 мл 35% раствора. Запах формалина в больших концентрациях также может вызывать аллергическую реакцию.
Формалин – прижигающий, дезинфицирующий, антисептический, дезодорирующий лекарственный препарат.
Лекарственная форма Формалина
Лекарственное средство – это прозрачная жидкость, которая имеет резкий специфический запах.
Раствор Формалина включает в себя 40 процентов формальдегида, 52 процента воды и 8 процентов метилового спирта. Формальдегид – это активное вещество препарата, который обладает дезодорирующими и дезинфицирующими свойствами.
Кроме этого применение Формалина эффективно для того, чтобы сохранять анатомические препараты.
Фармакологическое действие Формалина
По инструкции Формалин предназначен для свертывания белков, что нашло широкое использование его при сохранении, а также консервации различных биологических материалов, либо при применении в качестве антисептика.
Свойства Формалина полезны в производстве фенол-формальдегидных олигомеров.
Показания к применению Формалина
Раствор Формалина применяют в качестве дезодорирующего, а также дезинфицирующего вещества.
По инструкции Формалин широко используется при обмывании кожных покровов рук, ног, подмышечных впадин (если существуют признаки повышенной потливости – гипергидроз). Кроме этого лекарственное средство используют при сильно выраженном запахе пота.
Свойства Формалина активно применяют для дезинфекции различного медицинского оборудования, а также для стерилизации предметов, предназначенных для ухода за больными.
Существует множество лекарственных средств, которые созданы на основе раствора. К примеру, существует паста Теймурова. Данная паста используется для лечения опрелостей, определенных видов поражений кожных покровов, либо повышенной потливости.
Способ применения Формалина
Во врачебной практике для обмывания кожных покровов рекомендуется применять 0,5-2-процентный раствор Формалина. Для обмывания подошв специалисты назначают 3-5-процентный раствор.
По инструкции Формалин не следует использовать ежедневно, так как может произойти раздражение кожных покровов. Если у пациента обнаружены раздражения на теле, необходимо прекратить использование лекарственного средства, а воспаленные участки присыпать тальком.
Свойства Формалина помогают лечить микозы, грибковые заболевания стоп. Данным раствором специалисты советуют обеззараживать обувь и стельки: внутреннюю поверхность стельки необходимо протирать 25-процентным раствором, далее обувь следует 2 часа проветривать, пока не выветрится резкий и неприятный запах.
Противопоказания
По инструкции Формалин категорически запрещено применять при беременности, а также в период лактации. Объясняется данный запрет тем, что препарат является токсичным соединением, а также оказывает раздражающее действие на ткани.
Побочные эффекты
В основном при длительном применении Формалина в высоких концентрациях возникали раздражения на коже.
Отравление Формалином
При отравлении лекарственным средством пациент чувствует резкое жжение по ходу пищевода, а также в желудке. Помимо этого возникает рвота, которая сопровождается кровянистой массой, возникают головокружения, расстройства дыхания и сердечной деятельности. В некоторых случаях человек может потерять сознание.
Смертельная доза лекарственного средства составляет 10-20 миллилитров.
При вскрытии пациента наблюдается следующее: слизистая оболочка пищевода, желудка, рта достаточно уплотнена, фиксирована и имеет буровато-серый цвет. Желудок и петли верхнего отдела тонких кишок в виде петли плотной трубки имеют серый цвет снаружи, с хорошо выраженной складчатостью.
Помимо этого наблюдается сильный отек легких и мозга (что объясняет вышеперечисленные симптомы отравления), полнокровие внутренних органов. При вскрытии чувствуется резкий запах Формалина от полостей и органов.
Срок годности и условия хранения
Хранить лекарственное средство необходимо только в защищенном от света месте. Оптимальная температура для Формалина – комнатная.
"...Формалин представляет собой 35 - 40-процентный водный раствор формальдегида. При действии формалина на бактериальную клетку происходит денатурация (свертывание) белков клетки. В 5-процентном растворе формалина споровые формы погибают через 30 мин., в 2-процентном растворе - через 60 мин., в 1-процентном - через 2 ч. Для дезинфекции применяется формалин в виде 2-процентного раствора для обработки стен и потолков производственных помещений. Если имеется плесень, обработку производят 2 - 3 раза в месяц. Кроме того, его применяют для дезинфекции воздуха производственных помещений. Опрыскивание помещений рекомендуется делать после работы, чтобы запах успел выветриться. На 1 куб. м помещения требуется 25 мл формалина. Температура помещения должна быть не ниже 17 - 18 `C. С повышением температуры бактерицидное действие формалина повышается. Время экспозиции - не менее 5 ч. Из дезинфицируемого помещения необходимо убрать пищевые продукты. После окончания дезинфекции воздух помещений нейтрализуют 20-процентным раствором хлористого аммония (15 мл на 1 куб. м) в течение нескольких часов. Недостатком формалина является его токсическое действие на слизистые оболочки человека..."
Источник:
"Санитарные правила для предприятий маргариновой промышленности" (утв. Главным государственным санитарным врачом СССР 30.12.1971 N 946-А-71)
- - водный р-р формальдегида, хим. препарат для защиты р-ний от болезней, вызываемых фитопатогенными грибами и бактериями, антисептич. средство...
Сельско-хозяйственный энциклопедический словарь
- - бесцветная, прозрачная, сильно пахучая жидкость, водный раствор газа формальдегида...
Сельскохозяйственный словарь-справочник
- - формоль, - водный р-р, содержащий обычно 37 - 40% формальдегида и 6 - 15% метилового спирта; плотн. 1076 - 1100 кг/м3. Дезинфицирующее и дезодорирующее средство, источник формальдегида...
Большой энциклопедический политехнический словарь
- - formalin - .Водный раствор формальдегида; Ф. широко применяется как фиксатор, а также входит в состав различных составных фиксаторов; механизм фиксирующего действия Ф. - образование поперечных сшивок между белками...
Молекулярная биология и генетика. Толковый словарь
- - водный р-р, содержащий 37-40% формальдегида и 6-15% метилового спирта. При хранении мутнеет, т. к. выпадает белый осадок. Источник формальдегида, дезинфицирующее и дезодорирующее средство...
Естествознание. Энциклопедический словарь
- - 40% водный раствор альдегида муравьиной кислоты; обладает бактерицидным действием; в медицине применяется гл. обр. для дезинфекции...
Большой медицинский словарь
- - "... представляет собой 35 - 40-процентный водный раствор формальдегида. При действии формалина на бактериальную клетку происходит денатурация белков клетки...
Официальная терминология
- - см. Оксиметилен и Триоксиметилен...
Энциклопедический словарь Брокгауза и Евфрона
- - формоль, водный раствор Формальдегида, содержащий 4–12% метилового спирта в качестве стабилизатора; бесцветная жидкость со своеобразным острым запахом...
Большая Советская энциклопедия
- - водный раствор, содержащий 37-40% формальдегида и 6-15% метилового спирта. При хранении мутнеет, т. к. выпадает белый осадок. Источник формальдегида, дезинфицирующее и дезодорирующее средство...
Большой энциклопедический словарь
- - ...
Орфографический словарь русского языка
- - ФОРМАЛИ́Н, -а, муж. Дезинфицирующий и консервирующий раствор с острым запахом...
Методические указания.
Формалин – водный раствор формальдегида (35-40 %-ный). Он представляет собой бесцветную прозрачную жидкость с характерным запахом, при хранении в охлаждённом состоянии формалин мутнеет с образованием осадка. Для дезинфекции готовят раствор с определённым содержанием формальдегида в формалине.
Перед дезинфекцией необходимо проверять процентное содержание формальдегида в растворе. Обычно раствор формальдегида готовят из формалина, содержащего 35-40 % формальдегида. Например, чтобы приготовить 4 %-ный раствор формальдегида из имеющегося 40 %-ного формалина нужно вначале составить следующую пропорцию:
100: 40 = х: 4, откуда х = 100 ∙ 4 / 40 = 10
Найденная величина означает, что для получения 4 %-ного раствора формальдегида нужно взять 10 мл имеющегося 40 %-ного формалина и 90 мл воды.
На каждую партию формалина должен быть паспорт, в котором указывается название препарата, наименование завода, масса и процентное содержание формальдегида.
Формалином дезинфицируют объекты животноводства. Его можно применять в водных растворах, газообразном состоянии (пароформалиновые камеры, аэрозоли) как в чистом виде, так и в смеси с другими химическими средствами. Бактерицидное действие основано на способности формальдегида денатурировать микробные белки.
Задание 1. Определение процентного содержания формальдегида в формалине (метод титрации)
Посуда и реактивы: колба коническая на 500 мл, бюретки, нормальный раствор натра едкого, децинормальный раствор йода, децинормальный раствор натрия тиосульфата, хлористоводородная кислота – 1 н. раствор, 1 %-ный раствор крахмала.
Ход определения: в коническую колбу вливают 30 мл нормального раствора натра едкого, 50 мл разбавленного в 20 раз формалина (к 5 мл формалина добавляют 95 мл дистиллированной воды) и 100 мл 0,1 н. йода, который приливают из бюретки небольшими порциями, осторожно круговыми движениями колбы смешивая прилитую порцию йода с имеющейся в колбе жидкостью. Затем колбу закрывают пробкой и ставят в темное место на 30 минут, после чего добавляют 40 мл 1 н. раствора хлористоводородной кислоты. При этом почти бесцветная жидкость (смесь) становится бурой. Её титруют децинормальным раствором тиосульфата. Когда смесь станет слабо-желтой, в колбу вливают 1мл 1 %-ного раствора крахмала (индикатор). Жидкость приобретает синий цвет, а затем при продолжении титрования обесцвечивается. Процентное содержание формальдегида в формалине определяют по формуле:
х = (100 – y) ∙ 0,0015 ∙ 20 ∙ 20,
100 – количество раствора йода, мл;
у – количество тиосульфата, пошедшего на титрование, мл;
0,0015 – граммэквивалент формальдегида;
20 – разведение формалина;
20 – множитель для перевода в проценты.
Задание 2. Определение формальдегида в формалине по плотности
Посуда и реактивы: стеклянный цилиндр на 0,5 или 1 л, денсиметр с делениями 1,08-1,16, испытуемый формалин (должен иметь температуру 18…20 0 С).
Ход определения: формалин наливают в стеклянный цилиндр до ⅔ его высоты и денсиметром определяют его плотность. Процентное содержание формальдегида рассчитывают по формуле:
х = 1000 (D - 1) / 2,5,
D - плотность формалина;
1 - плотность воды;
1000 - множитель для перевода дробных чисел в целое;
2,5 - константа.
Сухой формалин (параформ) содержит 95-96 % формальдегида. Он представляет собой порошок белого цвета. Для получения раствора 1 %-ной концентрации берут 1 часть сухого формалина и 99 частей воды (для 3 %-ной концентрации соответственно 3 части порошка и 97 частей воды и т.д.). Вода должна быть подогрета до 50…60 0 С.
Растворы из сухого формалина применяют для дезинфекции в том же порядке и тех же концентрациях, что и растворы формальдегида.
Парасод и фоспар представляют собой порошки белого цвета, хорошо растворимые в горячей воде (50…60 0 С), устойчивые при хранении. Они готовятся на основе параформа, карбоната натрия и тринатрия фосфата и содержат 50 % параформа. Обладают высокими бактерицидными и вирулицидными свойствами. Для влажной дезинфекции применяют 3-4 %-ные растворы парасода и фоспара.
Для получения растворов такой концентрации берут соответственно 3 или 4 кг одного из препаратов постепенно добавляют 50 л горячей воды (50…60 0 С), перемешивая до полного растворения, затем доливают холодную воду до получения 100 л дезинфектанта.
При аэрозольном методе парасод и фоспар применяют в форме 40 %-ных растворов из расчета 30 мл на 1 м 3 помещения. Для приготовления 40 %-ных растворов берут 40 кг одного из препаратов на 100 л воды.
библиографическое описание:
Фиксация гистологического и биопсийного материала — .
код для вставки на форум:
Фиксация гистологического и биопсийного материала — .
wiki:
— .
ОБЩИЕ ПРИНЦИПЫ ФИКСАЦИИ
Фиксация обеспечивает стабилизацию тканевых структур иихуплотнение, прекращает аутолиз, стабилизирует локализацию структур. Механизм действия фиксаторов основан на коагуляции белков и стабилизации липидов. Для достижения этой цели возможны 3 подхода:
1. Высушивание
2. Замораживание
3. Химическая фиксация:
· Альдегиды (формальдегид, глутаровый альдегид)
· хромовая кислота
· тетраоксид осмия
· спирты (этанол, метанол)
· соли ртути (сулема)
Мы рассмотрим третий вариант. Прижизненно взятая ткань должна быть зафиксирована на протяжении (не больше)30-90 минут, температура фиксатора – 0-4С
Фиксация всегда приводит к большим или меньшим изменениям структуры и объема ткани, степень выраженности которых зависит от рН фиксатора, его концентрации, температуры, продолжительности воздействия и других факторов. Концентрация ионов водорода фиксатора должна соответствовать таковой в тканях, поэтому фиксатор должен иметь рН, близкий к нейтральному. Увеличение температуры фиксатора ускоряет процесс, но вызывает еще большие изменения в тканях. Слишком продолжительная фиксация приводит к значительному уплотнению материала, что в дальнейшем затрудняет его обработку. Для каждого конкретного вида исследования подбирают наиболее приемлемый фиксатор.
Полноценная фиксацияматериала обеспечивается при соблюдении ряда требований .
1. После вырезки кусочка ткани его немедленно погружают в фиксатор.
2. Объем фиксатора должен превышать объем фиксируемого материала в 10-20 раз, так как тканевая жидкость может существенно изменить концентрацию фиксатора.
3. В том случае, если цвет фиксатора изменяется после погружения в него кусочков ткани, фиксатор необходимо немедленно сменить.
4. Недопустимо повторное использование фиксаторов.
5. Для каждого фиксатора следует соблюдать установленное время фиксации. Длительное пребывание материала возможно лишь в некоторых фиксаторах, например 10 % нейтральном формалине, жидкости Боуэна.
Для фиксации лучше использовать емкости с широким горлом, чтобы не возникло проблем с извлечением фиксированного материала. Равномерность фиксации некоторых рыхлых тканей, например легочной, достигается помещением их на дно банки, а поверх них - прокладки из слоя марли или ваты.
Чаще материал фиксируют при комнатной температуре, но для некоторых видов исследования (гистохимических, электронно-микроскопических и др.) необходимо проводить фиксацию при 4°С. Материал срочных биопсий фиксируют при повышенной температуре фиксатора.
В экспериментальных исследованиях применяют также прижизненный перфузионный метод фиксации и его сочетание с обычным погружением в фиксирующую жидкость.
ПРОСТЫЕ ФИКСИРУЮЩИЕ ЖИДКОСТИ
Химическая фиксация:
· альдегиды (формальдегид, глутаровый альдегид)
· хромовая кислота
· тетраоксид осмия
· спирты (этанол, метанол)
· соли ртути (сулема)
· кислоты (уксусная, трихлоруксусная, пикриновая, азотная)
1. Альдегиды
Можно хранить месяцами, надо всего лишь контролировать рН.
Формалин. Основным, широко применяемым фиксатором служит формалин, представляющий собой 40% раствор формальдегида. Формальдегид – это газ, растворимый в воде до концентрации40% по массе, каким он и поступает в продажу под названием «Формалин ». В гистологической практике используют 10% раствор формалина, что соответствует 4% формальдегиду.
Из формальдегида готовят нейтральный (забуференный до рН 7,0) 10-12% формалин. Для этого в банку с 40% формалином засыпают карбонат кальция или магния либо смесь этих солей - доломит из расчета 100 г на 1 л формалина. Для получения 10 % нейтрального формалина через 24 ч к 1 части 40% нейтрального формалина добавляют 9 частей водопроводной воды. Продолжительность фиксации 24-48 ч при 20°С
В водных незабуференных растворах Ф-д со временем превращается в муравьиную кислоту, метиловый спирт и ацетон, которые ухудшают качество фиксации, как и выпадение белого осадка параформальдегида. В результате точную Со Ф-да в растворах формалина установить не представляется возможным. Если на дне банки с 40 % формалином образовался осадок белого цвета (параформальдегид), то его можно растворить, подогрев до 70-80° С (в вытяжном шкафу!), и использовать для фиксации. Очищенный коммерческий параформальдегид применяют как составную часть многих фиксаторов для гистохимических и электронно-микроскопических исследований.
Фиксатор может показывать себя не с лучшей стороны из-за примесей, в основном метанола(до16%).Для этого существуют методы приготовления свободного от метанола
4% ф-д по Гайеру
· 2гр параформальдегида + 50мл 0,1М фосфатного буфера(рН 7,4-7,6)=нагревают до 70с до просветления раствора, помешивают, охлаждают и фильтруют. Его рН 7,3-7,5.
40% ф-д по Глауерт
· готовят 40% параформальдегид(40гр порошка формальдегида + 100мл дистиллированной воды при нагревании до 65С, перемешивая.
Несколько капель 40%гидроксида натрия до просветления раствора.
Солевой формол.
· Нейтральный 40% формалин 100 мл
· Хлорид натрия 8,5 г
· Водопроводная вода 900 мл
Продолжительность фиксации 48 ч при 20 ° С с последующей промывкой в проточной воде в течение 6-12 ч.
Универсальным фиксатором, пригодным для гистологических и большинства гистохимических исследований, является нейтральный формалин по Лилли ).
1. А. 100 мл 40 % формалина + 900 мл дистиллированной воды.
2. Б. 4 г дигидроортофосфата натрия моногидрата (однозамещенного фосфата натрия).
3. В. 6,5 г гидроортофосфата натрия (двузамещенного фосфата натрия).
Фиксатор Лилли для кислых гликозаминогликанов
1. Нитрат свинца 8гр
2. 40% раствор формальдегида 10мл
3. вода 10мл
4. этанол 80мл
продолжительность фиксации 24 часа при комнатной Т(при 4С – 2-3дня, 10-14 дней при –25С).
1. Пикриновая кислота, насыщенная в 96% спирте 85 частей
2. Раствор формальдегида 40% 10 частей
3. Ледяная уксусная кислота 5 частей
Глутаровый альдегид для ферментов.
Обеспечивает наибольшую сохранность ферментов.
· 0,2М фосфатный или какодилатный буфер(рН 7,2-7,4) 50л
· 25%глутаровый альдегид 10мл
· сахароза 8,5гр
2.Тетраоксид осмия.
Приводит не коагулируются, а желатинизируются, ткани не сморщиваются. Одновременно является контрастирующим веществом в электронной микроскопии. Дорогой реагент, поступает в продажу в ампулах по 0,5 – 2 гр. Разбивают в бумаге и помещают в
воду больше 24ч для 1-4 % раствора. Хранят в темноте при комнатной температуре месяцами. Для первичной фиксации липидов используют 1% раствор на 0,1М фосфатном буфере. Для 1 фиксации
· 2% ТО в ДВ 5мл
· натрия хлорид 850мг
· 0,2М фосфатный буфер 5мл
Для вторичной используют сахарозу вместо натрия.
Раствор Флеминга
· 2% ТО на дв 2мл
· 1% раствор хромовой кислоты на дв 7,5мл
· ледяная уксусная кислота 0,5мл (смешивать перед использованием)
3.Хромовая кислота.
Для стабилизации липидов, для фиксации гликогена и нуклеиновых кислот.
Фиксатор Элфтмана (бихроматсулема)
· Сулема 5 гр.
· Бихромат калия 2,5 гр.
Продолжительность фиксации 3 дня.
4.Этиловый спирт (80 %, 90 %, 96 % и 100 %).
Его применяют для осаждения белков, в качестве фиксатора для выявления гликогена, железа, амилоида, но он растворяет липиды. Механизм действия основан на осаждении белков, при этом происходит обезвоживание объектов, что значительно ускоряет проводку. Продолжительность фиксации от 2ч до 1 суток. Увеличение длительности фиксации, особенно в 100 % спирте 1 , нежелательно, так как материал значительно уплотняется и происходит его пересушивание. Оптимальная температура для фиксации материала в спирте +4 °С, но ее можно проводить и при комнатной температуре. Если после спиртовой фиксации предстоит резать ткань на замораживающем микротоме или криостате, то кусочки промывают в течение 1 -2 ч до их полного погружения на дно банки, при этом происходит насыщение ткани водой.
5.Уранилацетат
Используют в электронной микроскопии как третий фиксатор (после альдегида и тетраоксида осмия) и одновременно как контрастер. Хорошо выявляет мембраны благодаря стабилизации фосфолипидов, стабилизации ДНК.Применяют 0.25-2% в воде или в 50-70% спирте (окрашивание 8 минут).
Ацетон (его действие подобно действию спирта). Ацетон используют для увеличения скорости фиксации. Применяют 100% ацетон, для получения которого в коммерческий ацетон засыпают прокаленный сульфат меди (медный купорос) или силикагель. В ацетоне фиксируют кусочки толщиной 3-4 мм в течение 2 ч при 20° С или 30 мин- 1 ч в термостате при 60 °С в плотно закрытой посуде. Ацетон значительно уплотняет ткань и при увеличении продолжительности фиксации возможно сморщивание объектов. Чаще ацетон применяют для обработки материала срочных биопсий при его заливке в парафин.
6.Кислоты.
Азотная, пикриновая, уксусная, трихлоруксусная. Быстро проникают, препятствуют сморщиванию,
ослабляют состояние гидратации. Входят в состав декальцинирующих смесей.
Фиксатор Жандра для гликогена
4. Пикриновая кислота, насыщенная в 96% спирте 85 частей
5. Раствор формальдегида 40% 10 частей
6. Ледяная уксусная кислота 5 частей
Жидкость Буэна
классический фиксатор для экспериментальных исследований.
· Насыщенный раствор пикриновой кислоты 75 мл
· Нейтральный 40 % формалин 25 мл
· Ледяная уксусная кислота 5 мл
Продолжительность фиксации 1-24 ч при 20 °С. Насыщенный раствор пикриновой кислоты готовят заранее из расчета 3 г кристаллической пикриновой кислоты на 1 л горячей дистиллированной воды. После фиксации кусочки отмывают от избытка пикриновой кислоты в 70 % спирте, затем заливают в парафин.
Жидкость Карнуа
универсальный фиксатор для большинства гистологических и гистохимических исследований (кроме выявления липидов). Наилучший для кожи, для предупреждения пересушивания в качестве промежуточной среды используют хлороформ.
· Спирт 100 % или 96 % 60 мл
· Хлороформ 30 мл
· Ледяная уксусная кислота 10 мл
Продолжительность фиксации 2-4 ч при 4 ° С или 1-2 при 20 °С. Затем материал помещают в 100 % спирт. Если материал не сразу подлежит проводке, то его можно перенести 96 % спирт и держать в нем до 3 суток.
Сюда также входят фиксирующие смеси по Боуену, Жандру, Карнуа, Лилли, Ценкеру, Бродскому, прочее.
7.Сулема (дихлорид ртути).
Сулему применяют в качестве фиксатора с начала развития гистологии. Готовят насыщенный раствор: 10 г сулемы на 100 мл дистиллированной воды или изотонического раствора хлорида натрия доводят до кипения, охлаждают, фильтруют. Продолжительность фиксации кусочков толщиной 3 мм 6-12 ч при 20 °С. При фиксации сулемой возможно появление в тканях кристаллического осадка, который удаляют путем обработки срезов йодированным 70 % спиртом (на 50 мл 70 % спирта - 5-10 капель 5 % спиртового раствора йода до появления оранжевого цвета). По мере обесцвечивания йодированного спирта со срезами его заменяют свежей порцией вплоть до полной потери цвета, затем срезы промывают в 3-4 сменах 70 % спирта.
СЛОЖНЫЕ ФИКСАТОРЫ
Составными частями сложных фиксаторов являются простые. Существует множество вариантов фиксирующих смесей. Ниже приведены наиболее распространенные.
Спирт-формол по Шаферу.
· 10 % нейтральный формалин, который готовят из 1 части нейтрального 40 % формалина и
· 2-3 частей 96 % спирта.
Продолжительность фиксации 24-48 ч. Дальнейшая промывка в воде не требуется, и материал сразу же помещают в 96 % спирт.
Кальций-формол по Бейкеру (Проверено) используют для фиксации липидов.
· 10 мл 40% формалина + 90 мл дистиллированной воды.
· 1 г хлорида кальция.
Растворы смешивают.
Продолжительность фиксации 24-48 ч при 20°С.
Для гистохимических исследований с успехом применяют фиксатор Бейкера , приготовленный из параформальдегида.
· К 50 г параформальдегида и 500 мл дистиллированной воды добавляют с одновременным встряхиванием несколько капель 1 н. гидроксида натрия до исчезновения осадка.
· 10 г хлорида кальция + 500 мл дистиллированной воды.
Растворы А и Б смешивают, добавляют 0,5 г активированного угля. Перед использованием фильтруют.
Продолжительность фиксации 24-48 ч при 20°С.
Используется также фиксатор Карнуа , в состав которого входят
· 75 мл 100 % спирта
· 25 мл ледяной уксусной кислоты
Условия фиксации те же. В случае отсутствия этилового спирта вместо жидкости Карнуа можно использовать смесь следующего состава:
· Изопропиловый спирт 60мл
· Пропионовая кислота 30м
· Ацетон 10мл
· Диоксан 10мл
Продолжительность фиксации 12-24 ч при 20 °С; для промывки и обезвоживания применяют изопропиловый спирт.
Жидкость Ценкера - сулемовая смесь.
· Бихромат калия 2,5г
· Сульфат натрия 1 г
· Дистиллированная вод100мл(это-жидкость Мюллера).
· Сулема 5г
· Ледяная уксусная кислота 5мл
Ледяную уксусную кислоту можно заменить нейтральным 10 % формалином (фиксатор Максимова, ценкер-формол). Продолжительность фиксации 1-24 ч при 20°С. После фиксации материал в течение 12-24 ч отмывают в проточной воде и помещают в йодированный 70% спирт для удаления остатков сулемы. При добавлении 10 мл 2 % раствора тетраоксида осмия хорошо фиксируются и окрашиваются липиды.
В последнее время для гистологических исследований часто применяют глутаровый альдегид, параформальдегид, фиксаторы Ито, Замбони и др., особенно в тех случаях, когда материал предназначается одновременно для нескольких видов исследования (иммуноморфологического, электронно-микроскопического), а его количество ограничено, например, при пункционных биопсиях.
ПРАВИЛА РАБОТЫ С ФИКСАТОРАМИ
Практически все фиксаторы относятся к токсичным веществам (альдегиды, ацетоны, спирты), некоторые ядовиты (сулема, тетраоксид осмия, метанол), поэтому необходимо соблюдать правила техники безопасности при работе с реактивами, которые используют в гистологической практике.
Фиксацию и вырезку материала необходимо производить в вытяжном шкафу. Материал, извлеченный из фиксатора, содержащего формалин, желательно в течение нескольких минут промыть в проточной воде, так как пары формалина оказывают раздражающее действие на слизистые оболочки глаз и органов дыхания.
БЫСТРАЯ ФИКСАЦИЯ МАТЕРИАЛА СРОЧНЫХ БИОПСИЙ
Доставленный в лабораторию материал в случае необходимости вырезают или разрезают на несколько кусочков и фиксируют с помощью одного из способов быстрой фиксации. Если возможно, то следует часть материала сохранить для изготовления постоянных препаратов.
1. Материал помещают в металлический сосуд с ручкой и заливают теплым 10% нейтральным формалином, доводят до кипения, затем промывают проточной водой в течение 2-5 мин и режут на замораживающем микротоме или криостате.
2. Кусочки фиксируют в 100 % ацетоне в термостате при 56°С в течение 15 мин, затем помещают в хлороформ или ксилол для последующей заливки в парафин.
3. Материал фиксируют в смеси 10 % нейтрального формалина и 96 % спирта (1:1) в течение 15 мин при 56°С, затем промывают в 96 % спирте и обезвоживают в 100 % спирте.
4. М. Vinci и соавторы (1990) предложили метод фиксации кусочков ткани объемом 0,5-1 см 3 с применением микроволновой техники. Материал в растворе альдегида помещают на 20с в микроволновуюпечь (2,5 Гц/500 В), а затем оставляют на 10- 30 мин при комнатной температуре в том же фиксаторе. Микроволновое излучение способствует быстрому проникновению альдегидов в клетки и ткани, в результате чего улучшается качество фиксации. Этот способ позволяет проводить не только обычные гистологические, но и ультраструктурные цитохимические, иммуноморфологические исследования, а также рентгенологический микроанализ.
ВОЗМОЖНЫЕ АРТЕФАКТЫ, СВЯЗАННЫЕ С ФИКСАЦИЕЙ, И ИХ УСТРАНЕНИЕ
При фиксации формалином, особенно кислым, возможно появление в срезах темно-коричневого пигмента в виде зернышек или глыбок (результат реакции формалина с гемоглобином ткани). Пигмент удаляют, помещая срезы на 15-20 мин в 1-5 % раствор аммиака или 70 % спирт. После промывания водой препарат можно окрашивать. Хорошо удаляется пигмент в растворе 1 % гидроксида калия в 80 % спирте (1:25): после 10-минутной экспозиции препарат промывают в проточной воде в течение 5 мин.
В случаях значительного уплотнения ткани в результате слишком продолжительной фиксации кусочки помещают на 1-2 ч в 10% раствор лимонной кислоты, в результате чего материал становится более мягким и пригодным для исследования.
Кристаллический осадок, образующийся после фиксации с применением сулемы, удаляют из кусочков или лучше срезов с помощью йодированного 70 % спирта.